电池以化学能的形式储存电能,化学能可以转化为电能。化学能转化为电能的过程称为放电。放电过程中的化学反应使电子流过连接到终端的外部负载,导致电子流向相反方向。 有些电池可以通过施加反向电流将电子返回到同一个电子,称为充电。可以在同一电极上回收电子的电池称为可充电电池,如果不能,则称为不可充电电池。 在电池中,还原电极称为阴极,氧化电极称为阳极。 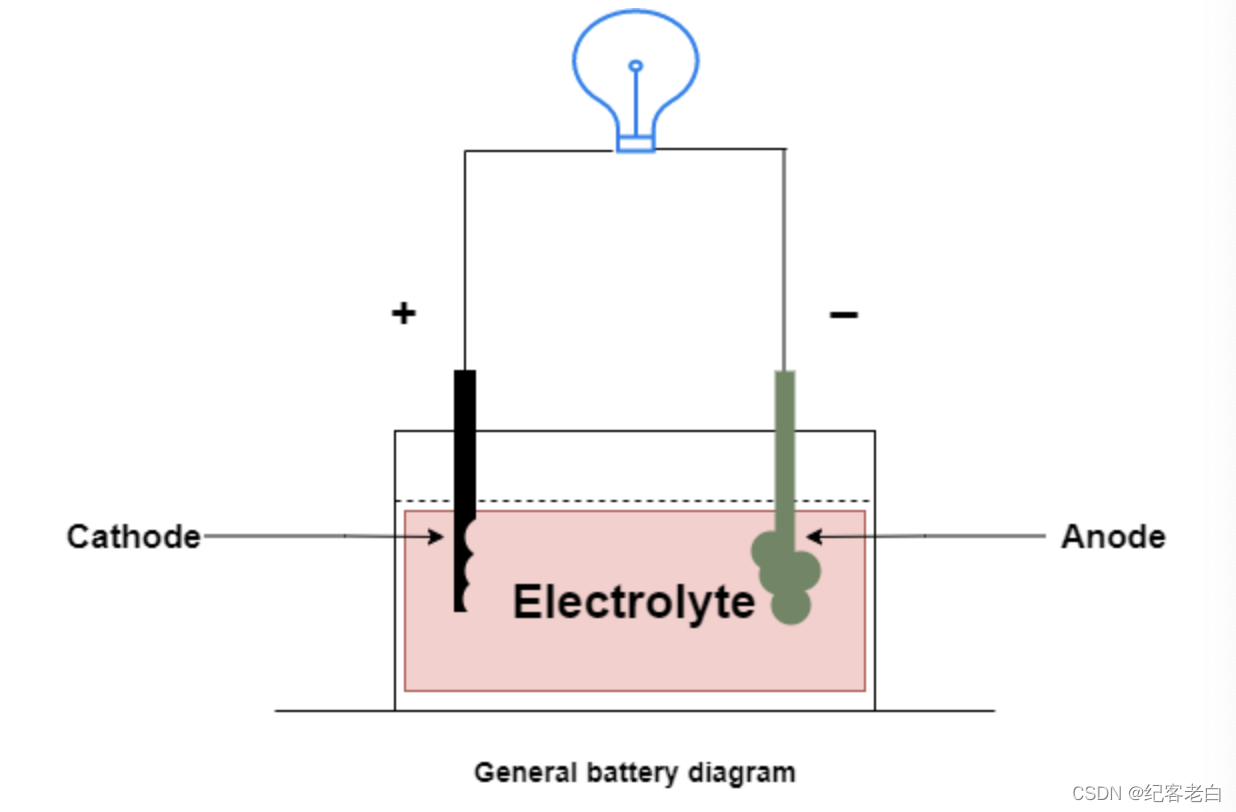
市场上常用的充电池有三种。
- 铅酸蓄电池
- 镉镍电池
- 镍氢电池
- 锂离子电池
铅酸蓄电池
首先,铅酸电池是1859年由法国物理学家制成的 Gaston Plante 发明。负极(阳极)是由海绵或多孔铅组成的。正极(阴极)由氧化铅组成。阳极和阴极电极浸泡在硫酸和水(稀硫酸)的电解质中。
放电铅酸电池
Pb HSO4-ーーーー > PbSO4 h 2e- 负电极上的反应 PbO2 HSO4- 3H 2e-ーーーー > PbSO4 2H2O 正电极上的反应 总反应 Pb PbO2 2h2so4ーーーー > 2PbSO4 2H2O
硫酸铅电池在正极(阴极)和负极(阳极)上的放电(PbSO4)由于铅价电荷的变化,晶体的形成释放电子。硫酸盐是电池中的电解液。这使得硫酸在充分放电时浓度较低,两个电极都被硫酸铅和水覆盖,电极周围没有硫酸。全放电时,电极完全覆盖同一材料,材料为硫酸铅,因此两个电极之间没有化学电位或电压。在实践中,早在这一点之前,就有一个停止放电的截止电压。 让我们来看看放电率。铅酸电池通常指定为8、10或20小时 c/8,c/10,c如果你发现电池120v 200Ah/10h 或 c/10。 c/10 = 200 Ah/10 h = 20A 该 c/10米电压切断后的特定时间为10小时 c/10。
充电铅酸电池
充电开始时,充电器连接到前端和负端。铅酸电池将硫酸铅带到负极(PbSO4)转化为铅(Pb) ,硫酸铅在正极(PbSO4)转化为氧化铅。化学反应在放电过程中逆转
充电铅酸电池
PbSO4 2H2O 正电极上的反应ーーーーー > PbO2 HSO4- 3H 2e- PbSO4 h 2e-ーーーーー > Pb HSO4- 负电极上的反应 全反应2pbso4 2H2O ーーーーー > Pb PbO2 2H2SO4 充电电流从电解质中电解水,氢气和氧气产生这个过程,称为电池的气体。这种气体排放会导致电池出现几个问题。由于产生的氢具有爆炸性,这是不安全的。这也减少了电池中的水,可以手动更换,但它增加了一个维护因素。气体排放可能会导致电解质中活性物质的屏蔽,从而永久降低电池容量,这就是为什么电池不应定期超过导致气体排放的电压。放气电压可以随充电速率而变化 铅酸蓄电池的充电方法有多种。但是我们应该采用最好的方法来减少放气的机会,以获得最大的电池使用寿命和容量。下面给出的方法列表。
- 恒压:-作为名称,该方法将提供恒压,直到电池电流为零。这需要很长时间
- 恒流:-作为名称,该方法将提供恒定电流,直到电压达到规定的放气电压。这也需要很长时间。
- 多级恒流充电电流:-在这种方法中,当电压达到放气电压时,充电电流保持恒定,然后电流开始逐渐降低,以保持电压低于放气电压。这个充电器很复杂。
- 改进的恒压恒流:-在这种方法电池充电三个阶段。第一阶段是恒流阶段,在这个电流施加到电池直到电压达到其规定的放气电压。在第二阶段,电压保持不变,直到电流减小到0.1 c20左右(也叫 C20/10).25 v 到2.27 v) ,保持电池充电。 在电池标签上可以找到充电电流和充气电压,就像你可以看到图中有两种模式可以选择充电电压和电流一样,即待机和回收。循环利用是指使用需要快速充放电的电池。待机使用是指电池已充电并在必要时使用。0.1 c 意味着0.1乘以电池总容量。假如你有40ah 电池,那么0.1 c 就是0.1 x 40 = 4 a。0.25 c = 0.25 x 40 = 10A.
铅酸电池使用说明书 铅酸电池的寿命周期 铅酸电池的寿命取决于多种因素。一般来说,浅循环电池的充放电周期约为200ー300次,但这个数字可以增加或减少。该电池的寿命周期取决于三个因素: 放电深度,正确的充电周期和温度。深循环电池可以维持约1000个生命周期,但黄色循环和深循环是什么?你可以在下面找到它。
深度
放电深度(DOD)这意味着电池的放电量。假设你有100个ah 电池,你放电20分钟,50分钟A,因此,放电深度如下 隐蔽时间以小时计算。 = 20/60 计算排放时间 = 50x20/60 = 16.7 a 排放深度 = (排放量/容量) x100 = (16.7/100) x100 = 16.7% 按需分为两类,即按需50% 上述按需能力的电池, 深循环电池, 即使深循环电池的放电深度超过50% 它还可以保持约1000个寿命周期,而浅循环电池可以很好地保持其寿命周期,如下图所示。
浅循环电池容量、放电深度与循环寿命的关系 充电: 若充电不正确,则会导致过充或充电不足,这也会降低电池容量。
温度: 温度还会影响电池的使用寿命在低温运行时降低电池容量,增加电池的老化速度。
镉镍电池
首先,1899年由沃尔德玛制成的镉镍电池 · 由碱氧化镍发明的正极(阴极)(NiO (OH))金属镉(阳极)由金属镉制成(Cd)制作。使用的电解质是在蒸馏水中加入30% 氢氧化钾。电解质水平高于电极。电解质在充放电过程中没有明显变化。
镉镍电池放电
该电池的放电/充电周期约为2000次。 标称电压为1.2伏每个电池的充电电压为1.当电压降至155伏时,当电压降至15伏.1伏时完全放电,电压可串联电池增加电压。电池容量由制造商决定,一般 AA 电池容量接近1万mah。 镉镍电池放电 当负载连接到终端时,电池开始放电。氢氧化钾(KOH)氢氧化钾分解成钾离子和羟基离子。(OH -)离子向负电极移动。负电极释放电子,正电极通过外部连接接收电子。这导致电流通过负载从正极流向负极。 Cd 2OH ーーーー > Cd (OH)2 2e-负电极上的反应 NiO (OH) H2O 2e-ーーーーー > Ni (OH)2 OH-正电极上的反应 全反应 Cd 2NiO (OH) 2H2O ーーーー > 2Ni (OH)2 Cd (OH)2 放电速率随电池大小而变化,普通 AA 电池可以提供大约1.8安培电流,d 大小电池可提供约3个.5安培电流。 镉镍电池充电 充电时,充电器连接到终端。反应从放电反向进行。正极将氢氧化镍转化为氢氧化镍并释放电子。负电子从外部连接处获取电子,并将 Cd (OH)2转化为 Cd。
镉镍电池充电 Ni (OH)2 OH-ーーーーー > NiO (OH) H2O 2e-正电极上的反应 Cd (OH)2 2e-ーーーー > Cd 2OH 负电极上的反应 总反应2ni (OH)2 Cd (OH)2ーーー > Cd 2NiO (OH) 2H2O 充电周期结束时,电池会释放气体,当电池充电过多时也会发生。从这种气体中,电解质中的水分解成负电极中的氢和正电极中的氧。这种气体的沉淀取决于电池充电的电压和温度。镉和镍电池必须充满电并进行微量气体沉淀,以利用电解质浓度中的部分水。 镉镍电池有两种充电方式: 慢速充电和快速充电。
- 慢速充电:-慢速充电电流约为0.1 c,充满电后不会损坏电池。该方法还用于克服镍镉电池的自放电。
- 快速充电:-在快速充电时,电池以约1摄氏度的恒定电流充电。是电池的容量,如果你用的是4ah 电池,那么1c 意味着1 x 4 = 4A。一旦完全充电,可以通过下面给出的电荷检测算法检测到。电流将降低到0.1摄氏度,滴流充电。滴流充电是指以与电池自放电相同的速度充电。这将使电池充满电。 全电荷检测算法可以使用两个因素 v 或温度。 若采用温度检测算法,则快速充电时温度为45度,慢速充电时温度为50度。 在负增量 v 在检测算法中,充满电后电压下降。该液滴可用于检测全电荷状态。该方法称为负增量 v。该方法提供了精确的全电荷检测。 镍氢电池 首先,1967年,巴特尔-日内瓦研究中心发明了镍氢电池。三洋于2005年推出 Eneloop 品牌。在这种电池中,正极(阴极)是由碱氧化镍和负极(金属氢化物)制成的。电解质是用蒸馏水浓缩的氢氧化钾。
镍氢电池 该电池的放电/充电周期约为180-2000次。这取决于你如何充电或放电各种因素。 这种电池几乎类似于镉镍电池。镍氢电池的标称电压为1.2 v,用于单个电池。但当充满电时,电压为1.5 v,充满放电电压为1.0 v。电池的电流容量随其大小而变化,一节 AA 电池容量可接近2万mah。 镍电池的放电 当负荷连接到终端时,开始发生放电反应。金属氢化物(MH)与 OH 离子反应生成 m 和水,也释放出一个电子。电子被 NiO (OH)通过外加载荷带走。这导致电流通过负载。
镍氢电池的充电 MH + OH-ーーーーーーー > m + H2O + e-中的反应 NiO (OH) + H2O + e-ーーーーー > Ni (OH)2 + OH-正电极上的反应 总反应 NiO (OH) + MH ーーー > Ni (OH)2 + m 正常情况下,镍氢电池的放电速率为3c (其中 c 是电池的容量,但高品质的电池可以放电高达15c 的速率。 镍氢电池的充电 在充电时,充电器连接在电池的末端,充电反应与放电反应相反。正极将氢氧化镍转化为水,并释放出一个电子。这个电子被负电极从外部导线和它从 MH 再次。
镍氢电池的充电 Ni (OH)2 + OH-ーーーー > NiO (OH) + H2O + e-正电极上的反应 负极 m + H2O + e-ーーーーー > MH + OH-的反应 总反应 Ni (OH)2 + m ーーーー > NiO (OH) + MH 镍氢电池充电化学利用恒流和恒压算法,可分为四个部分给出如下。
- 充电:-当电池深度放电时,每个电池的电压低于0.9 v。用来给电池充电的最大恒定电流为0.1摄氏度,这种电流称为滴流充电。
- 恒流:-当每个电池的电压高于0.9 v 时,在0.2 c 到1c 范围内施加恒流来进行恒流充电。
- 充电终端:-充满电的电池可以检测到一个完整的充电检测算法,这是解释如下。充满电后,涓流充电按照自放电的速度使用,以保持电池充满电。 全电荷检测算法可以使用两个因素负增量 v 或温度。 如果该算法利用温度来检测,那么温度将在45度到50度之间检测到充满电。 在负增量 v 检测算法中,充满电后电压下降。这种液滴的检测可以用来检测全电荷状态。这种方法称为负增量 v。这种方法提供了精确的全电荷检测。
锂离子电池
首先,吉野彰在1985年开发了一个锂离子电池。正极(阴极)由锂钴氧化物制成,负极(阳极)由石墨制成。锂盐作为一种有机溶剂被用作电解质。分离器用来分离电极
锂离子电池 这种电池的放电/充电周期约为400-1200次循环。这取决于各种因素,你如何充电或放电的电池。 锂离子电池的额定电压为3.60 v。当电池完全充电时,电压约为4.2 v,当电池完全放电时,电压约为3.0 v。锂离子电池有不同的尺寸和形状,其容量也可根据需要提供。 锂离子电池的放电 在电池放电时,负载连接到终端电池。锂离子从负电极中释放出来,进入电解液中。这种锂离子被正电极吸收。负电极也释放穿过外部导线到正电极的电子。这给我们的电路提供了电流。
锂离子电池的放电 (锂离子电池放电) Lic6ーーーーー > C6 + Li + e-在负极上的反应 Coo_2 + Li + e-ーーーー > licoo_2正电极上的反应 全反应 LiC6 + coo_2ーーーーー > C6 + LiCoO2 锂离子电池可以以10c 的速率放电(其中 c 是电池的容量)。如果你的电池可以提供1000mah,那么放电速率将是10x1000 = 10000mAh。 锂离子电池的充电 锂离子电池充电时,电池与充电器连接。正电极损失一个带负电荷的电子。为了维持负电极上的电荷平衡,等量的正电离子溶解到电解质溶液中。这些锂离子移动到正极,在那里它们被石墨吸收。这种吸收反应也将电子沉积到石墨阳极上,以“束缚”锂离子。
锂离子电池的充电
Licoo2ーーーーーー > coo_2 + Li + e-正电极上的反应 C6 + Li + + e-ーーーー > lic6负电极上的反应 全反应 C6 + licoo2ーーーー > LiC6 + CoO2 锂离子电池充电化学使用恒流和恒压算法,可分为四个部分。 充电:-当电池深度放电时,每个电池的电量低于3.0 v。用来给电池充电的最大恒定电流为0.1摄氏度,这种电流称为滴流充电。 恒流:-当电压高于每个电池3.0 v 时,在0.2 c 到1c 范围内施加恒流进行恒流充电。 恒压:-当电压达到每个电池4.2 v 的恒流充电。恒定的电压直到电池的电流降为零,这最大限度地提高了电池的性能。 充电终止:-充电结束检测算法,检测当前范围下降到0.02 c 到0.07 c 或使用计时器方法。它检测当一个恒定电压阶段启动它终止充电器后2小时的恒定电压阶段。
-
白纪龙老师从事电子行业已经有15个年头, 到目前为止已开发过的产品超上百款,目前大部分都已经量产上市,
-
从2018年开始花了5年的时间, 潜心录制了上千集的实战级电子工程师系列课程, 该课程从元器件到核心模块到完整产品
-
老白的初心是“愿天下工程师 不走弯路” 其中, 就有详细讲解MOS管和IGBT的课程!